HIFU para Câncer de Próstata: Guia Completo do Paciente em 2026
Introdução
Receber o diagnóstico de câncer de próstata localizado costuma colocar o paciente diante de uma escolha tradicional: cirurgia, radioterapia ou vigilância ativa. Para muitos homens, nenhuma dessas opções parece perfeita — operar significa enfrentar incontinência e disfunção erétil, irradiar significa semanas de tratamento e efeitos tardios cumulativos, e apenas observar pode parecer arriscado quando o tumor já foi confirmado. É exatamente nessa lacuna que entra o HIFU.
O HIFU (High-Intensity Focused Ultrasound — ultrassom focalizado de alta intensidade) é um tratamento minimamente invasivo que destrói apenas a área do tumor dentro da próstata, preservando o restante do órgão e estruturas vizinhas críticas — esfíncter urinário, feixes neurovasculares, colo vesical e reto. Em 2026, depois de mais de 25 anos de evolução técnica e quase 15 anos de dados consolidados de seguimento, o HIFU é reconhecido pelas principais diretrizes mundiais (EAU 2025, NCCN 2026, AUA, ICTC) como uma opção válida para pacientes selecionados com câncer de próstata localizado.
Mas — e este "mas" é fundamental — o HIFU não é para todo mundo. Quando indicado para o paciente certo, oferece controle oncológico comparável à cirurgia e à radioterapia com preservação dramática da função sexual e urinária. Quando indicado para o paciente errado, perde seus benefícios e pode comprometer tratamentos futuros. A seleção criteriosa é tudo.
Este guia foi escrito para ser a referência mais completa em português sobre HIFU para câncer de próstata em 2026: como funciona, quem se beneficia, como é feito, o que esperar antes, durante e depois, quais resultados a literatura mostra, quais são as limitações reais que outros centros nem sempre discutem, e como se posicionar dentro das opções disponíveis. Leia com calma, anote suas dúvidas e leve este conteúdo para a sua consulta especializada.
1. O Que É HIFU e Como Ele Funciona?
O HIFU (High-Intensity Focused Ultrasound) é uma técnica que utiliza ondas de ultrassom de alta intensidade — semelhantes às usadas em exames de ultrassonografia, mas com energia milhares de vezes maior — focalizadas em um ponto preciso dentro da próstata.
O Princípio Físico — Analogia da Lupa
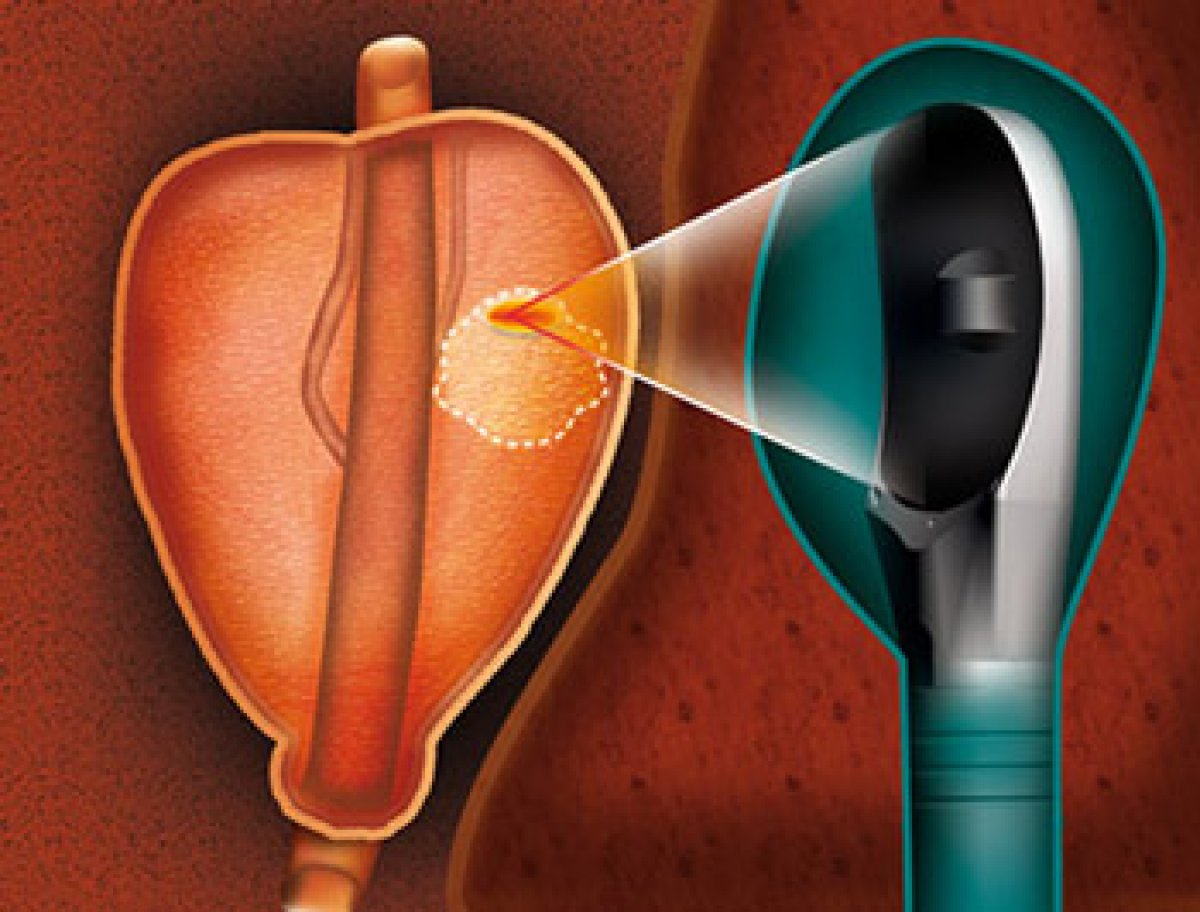
Imagine usar uma lupa para concentrar a luz do sol em um único ponto sobre uma folha de papel. Em segundos, a folha queima — não porque a luz mudou, mas porque sua energia foi concentrada em um foco preciso. O HIFU faz exatamente isso, mas com som em vez de luz e dentro do corpo, sem cortar nada.
O Que Acontece no Tecido
Quando as ondas de ultrassom são focalizadas, geram dois efeitos no ponto-alvo:
Efeito térmico: a temperatura sobe para 80-100°C em poucos segundos, causando necrose coagulativa — destruição celular irreversível por calor.
Efeito mecânico (cavitação): as ondas geram bolhas microscópicas que se expandem e colapsam rapidamente, contribuindo para a destruição do tecido.
Cada disparo de HIFU destrói um pequeno volume de tecido (poucos milímetros cúbicos) com precisão milimétrica. O cirurgião faz centenas a milhares desses disparos sobrepostos para cobrir toda a área-alvo, sob orientação de ultrassom em tempo real (e, em algumas plataformas mais modernas, ressonância magnética em tempo real).
Por Que É Diferente de Cirurgia e Radioterapia
Cirurgia: remove fisicamente a próstata inteira (e geralmente as vesículas seminais).
Radioterapia: irradia toda a próstata com radiação ionizante, em múltiplas sessões.
HIFU: destrói apenas a área tumoral dentro da próstata, preservando o restante do órgão, em uma única sessão (com possibilidade de retratamento se necessário).
O paciente sai com a próstata anatomicamente em parte preservada, sem incisões, com sonda vesical temporária — e, na maioria dos casos, sem o impacto funcional brutal das opções radicais.
2. Breve História: De Experimento a Tecnologia Madura
O HIFU foi proposto pela primeira vez nos anos 1940. Para câncer de próstata, os primeiros estudos clínicos relevantes começaram nos anos 1990 na França (grupo de Lyon, com a plataforma Ablatherm) e nos Estados Unidos (Sonablate).
Por muitos anos, o HIFU foi tratado como terapia experimental. A virada começou na década de 2010, com:
- Chegada da ressonância multiparamétrica (mpMRI) com classificação PI-RADS, permitindo localização precisa do tumor.
- Biópsia direcionada por fusão MRI/US, que mapeia a lesão índice.
- Plataformas de HIFU de segunda e terceira geração, com melhor controle dosimétrico (Sonablate, Focal One, Ablatherm).
- Acúmulo de séries de 10 anos de seguimento mostrando resultados oncológicos sólidos em pacientes selecionados.
Em 2015, o FDA aprovou o HIFU para ablação de tecido prostático nos EUA. Hoje, em 2026, o HIFU é realidade clínica em centros de referência no mundo todo, incluindo Brasil — embora ainda com disponibilidade limitada.
3. Tipos de Ablação por HIFU
Não existe "um HIFU" — existem várias estratégias de ablação, escolhidas conforme a localização e extensão da doença:
Ablação Focal Pura
Destrói apenas a lesão índice com margem de segurança ao redor. Indicada para tumores muito bem localizados em um quadrante específico.
Hemiablação
Trata toda uma metade (direita ou esquerda) da próstata, preservando a outra. Indicada para câncer unilateral com lesão índice clara — a estratégia mais comum em HIFU focal.
Ablação Subtotal (Subtotal Gland Ablation)
Destrói a maior parte da próstata, preservando uma faixa de tecido posterior ao reto e ao redor do esfíncter para minimizar complicações. Indicada para doença mais extensa ainda focal-elegível.
Ablação de Glândula Inteira (Whole-Gland HIFU)
Trata toda a próstata. Estratégia mais antiga, hoje cada vez menos usada como primeira opção (perde a vantagem funcional do HIFU focal e tem mais complicações).
HIFU de Salvamento (Salvage HIFU)
Indicado em recidiva local após radioterapia falha. Cenário específico, com perfil de risco diferente, em centros muito experientes.
A escolha entre essas modalidades depende de uma combinação de localização do tumor, extensão, função basal do paciente, anatomia da próstata e expertise do centro.
4. Para Quem o HIFU É Indicado: Critérios de Elegibilidade
Esta é a parte mais crítica do processo decisório. Indicação inadequada destrói os benefícios da técnica e pode comprometer tratamentos futuros. Pacientes adequados são selecionados por uma combinação rigorosa de fatores.
Critérios de Elegibilidade Ideal
✅ Câncer unilateral ou unifocal identificado à mpMRI (PI-RADS 4-5) e confirmado por biópsia direcionada por fusão.
✅ ISUP 2 (Gleason 3+4) com baixo volume — perfil mais comum de candidato. Pacientes selecionados com ISUP 1 (Gleason 6) clinicamente significativo ou ISUP 3 (Gleason 4+3) em casos cuidadosamente avaliados também podem ser candidatos em centros experientes.
✅ Volume da lesão índice < 1,5 cm³ (idealmente < 1 cm³).
✅ Próstata de tamanho compatível com a tecnologia escolhida (geralmente < 40-50 mL).
✅ Sem calcificações importantes que bloqueiem a passagem do ultrassom.
✅ Anatomia favorável — lesões em região posterior, lateral ou ápice são as mais acessíveis ao HIFU transretal.
✅ PSA inicial < 15-20 ng/mL (em geral; varia conforme protocolo).
✅ Expectativa de vida > 10 anos e estado funcional adequado.
✅ Função urinária e sexual basal preservada — a motivação principal para escolher HIFU em vez de radical é justamente preservá-las.
✅ Paciente disposto ao seguimento rigoroso (PSA seriado, mpMRI e biópsia de re-avaliação).
✅ Mapeamento adequado por mpMRI + biópsia por fusão confirmando ausência de doença clinicamente significativa fora da área a tratar.
Critérios Que NÃO Favorecem HIFU
❌ Câncer multifocal/bilateral significativo sem lesão dominante clara.
❌ Câncer de alto risco (ISUP 4-5 / Gleason 8-10) ou com fatores de agressividade molecular (carcinoma intraductal, mutação BRCA2 confirmada).
❌ Extensão extraprostática documentada ou invasão das vesículas seminais (pT3 já estabelecido por imagem).
❌ Próstata muito volumosa (>50-60 mL) com a tecnologia disponível.
❌ Calcificações prostáticas extensas bloqueando o ultrassom.
❌ Anatomia desfavorável — lesão muito anterior (em próstatas grandes, fora do alcance), íntima ao reto, ou em ápice extremo com risco para esfíncter.
❌ Paciente sem condições ou disposição para seguimento rigoroso.
❌ Expectativa de vida < 10 anos — nesse cenário, vigilância ativa ou radioterapia podem ser preferíveis.
❌ Disfunção urinária ou erétil grave pré-existente — pode mascarar benefício funcional.
A decisão final é sempre individualizada e multidisciplinar. Idealmente, dois ou três especialistas (urologista uro-oncologista, radio-oncologista e médico nuclear/radiologista experiente em mpMRI) avaliam o caso antes da indicação definitiva.
5. Avaliação Pré-HIFU: O Que Precisa Ser Feito Antes
A qualidade do tratamento depende da qualidade da avaliação prévia. Um HIFU bem feito começa semanas antes do dia do procedimento.
5.1 Imagem Pré-Tratamento
Ressonância multiparamétrica da próstata (mpMRI): OBRIGATÓRIA. Identifica e caracteriza a lesão índice, classifica em PI-RADS, mede volume, define localização e relação com estruturas vitais (esfíncter, reto, colo vesical).
Biópsia direcionada por fusão MRI/US: mapeia a lesão índice e amostra áreas adjacentes para confirmar que não há doença significativa fora do alvo.
Biópsia transperineal de mapeamento (em alguns centros): amostragem sistemática transperineal para garantir caracterização completa.
5.2 Avaliação Funcional Basal
Tudo o que se deseja preservar precisa ser documentado antes:
- Continência urinária: questionário ICIQ, número de absorventes (se houver), uroflowmetria, IPSS.
- Função erétil: questionário IIEF-5, ereções espontâneas, uso de medicação.
- Sintomas urinários: noctúria, urgência, jato urinário.
- Função intestinal: descartar doença anorretal ativa.
5.3 Avaliação Clínica Geral
- Anamnese completa, comorbidades, medicações (especialmente anticoagulantes/antiagregantes).
- Avaliação cardiovascular para anestesia.
- Hemograma, coagulograma, função renal.
- Urocultura (importante — qualquer infecção urinária ativa contraindica o procedimento).
5.4 Discussão Multidisciplinar
Idealmente, o caso é discutido em reunião multidisciplinar com urologista uro-oncologista, radio-oncologista, radiologista experiente em mpMRI e (quando indicado) geneticista oncológico. Segunda opinião especializada é fortemente recomendada antes de decidir por HIFU.
5.5 Conversa Aberta com o Paciente
Discussão honesta sobre:
- Benefícios reais esperados (com taxas, não apenas adjetivos).
- Limitações da técnica (necessidade de seguimento, possibilidade de retratamento).
- Alternativas e por que HIFU seria a escolha neste caso específico.
- Implicações para tratamentos futuros se houver recidiva.
6. O Procedimento Passo a Passo: O Que Acontece no Dia do HIFU
Manhã do Procedimento
Jejum de 8 horas antes da anestesia. Internação no hospital algumas horas antes. Preparo intestinal leve (enema) na maioria dos centros, para limpar o reto.
No Centro Cirúrgico
Anestesia: geral ou raquianestesia (depende do centro e do paciente). Procedimento dura tipicamente 1 a 3 horas.
Posição: litotomia (decúbito dorsal com pernas elevadas).
Inserção do transdutor: sonda retal contendo o emissor de ultrassom + sensor de imagem é introduzida no reto. Em algumas plataformas (Focal One), a ressonância magnética pré-operatória é fundida com a imagem em tempo real para guiar o planejamento.
Planejamento dosimétrico: o cirurgião delimita na imagem o volume-alvo a ser ablacionado, com margens de segurança. Estruturas críticas (esfíncter, reto, feixes neurovasculares) são identificadas e poupadas.
Disparos focalizados: o equipamento gera centenas a milhares de pulsos focalizados, cobrindo toda a área-alvo em sobreposição. Cada disparo dura segundos. Sensores de temperatura monitoram em tempo real.
Monitorização da parede retal: dispositivo de resfriamento protege o reto. Em casos com risco de lesão retal, espaçadores (hidrogel) podem ser usados.
Finalização: após cobrir todo o volume, o transdutor é removido. Sonda vesical é instalada.
Pós-Operatório Imediato
Sala de recuperação anestésica por algumas horas. Alta no mesmo dia ou em 24 horas, conforme protocolo do centro e estado clínico.
Sonda vesical mantida por 5-10 dias, dependendo do volume tratado e protocolo institucional. Antibiótico profilático prescrito por alguns dias.
7. Recuperação Após o HIFU: O Que Esperar nas Primeiras Semanas
Primeiros 7 Dias
- Sonda vesical ainda presente — orientações de cuidado (limpeza, hidratação, esvaziamento da bolsa).
- Desconforto perineal leve a moderado, controlável com analgésicos comuns.
- Hematúria leve (urina rosada) frequente nos primeiros dias — normal, autolimitada.
- Sangramento retal pequeno ocasional — também autolimitado.
- Atividade física limitada — caminhadas leves liberadas; sem esforço, sem dirigir.
Retirada da Sonda (Geralmente 5-10 dias)
- Realizada em consultório, com avaliação pós-miccional para confirmar bom esvaziamento vesical.
- Pode haver urgência miccional e polaciúria nos primeiros dias após retirada (devido a edema local). Costuma melhorar em 2-4 semanas.
- Hematúria pode persistir discretamente por mais alguns dias.
2-4 Semanas
- Retorno gradual a atividades normais — trabalho leve (geralmente já em 7-14 dias), exercícios moderados em 3-4 semanas.
- Atividade sexual pode ser retomada após 2-4 semanas conforme orientação médica.
- Função erétil pode estar transitoriamente afetada por edema local — melhora progressiva.
1-3 Meses
- Eliminação de "debris" tecidual pela urina ocasionalmente (pequenos fragmentos de tecido necrótico) — pode causar episódios curtos de urgência ou hematúria.
- Função urinária geralmente estabiliza em 4-6 semanas.
- Função sexual retorna ao padrão funcional definitivo em 3-6 meses.
A maioria dos pacientes está plenamente recuperada e retornando à rotina normal em 4-6 semanas.
8. Seguimento Após HIFU: Protocolo Estruturado
O seguimento pós-HIFU é diferente e mais intenso do que após cirurgia ou radioterapia — porque a próstata permanece e pode desenvolver doença residual, recidiva local ou novos focos.
PSA Pós-HIFU: Uma Cinética Diferente
Ao contrário da prostatectomia (onde o PSA deve ficar indetectável), após o HIFU algum PSA continua sendo produzido pela próstata remanescente. O comportamento esperado:
- Queda gradual do PSA nos primeiros 6-12 meses.
- Atingimento de um "PSA nadir" (valor mínimo) — geralmente entre 0,5 e 2,0 ng/mL.
- Estabilidade em torno desse nadir indica bom controle.
- Elevação progressiva (≥ nadir + 1,2 ng/mL — critério de Phoenix adaptado ou Stuttgart) indica possível falha e requer investigação.
Cronograma de Seguimento (Sugestão Padrão)
- PSA a cada 3 meses nos primeiros 2 anos, depois a cada 6 meses até 5 anos, depois anual.
- Ressonância multiparamétrica aos 6-12 meses pós-HIFU e periodicamente conforme protocolo.
- Biópsia de re-avaliação geralmente entre 6 e 12 meses pós-HIFU, mesmo com PSA e ressonância tranquilizadores — confirma ausência de doença residual no leito tratado e mapeia eventual nova lesão em áreas não tratadas.
- Avaliação funcional (questionários IIEF-5, ICIQ) a cada 6-12 meses.
Quando Suspeitar de Falha do HIFU
- PSA em ascensão progressiva acima do nadir + 1,2 ng/mL (critério Phoenix adaptado).
- Nova lesão suspeita na mpMRI de seguimento (PI-RADS 4-5 em área não tratada ou no leito ablacionado).
- Biópsia de re-avaliação positiva para câncer clinicamente significativo.
Importante: pequenas elevações de PSA não significam necessariamente falha — podem refletir inflamação, prostatite, manipulação recente ou crescimento benigno do tecido preservado.
9. Resultados Oncológicos do HIFU: O Que a Evidência Mostra
Com mais de 15 anos de dados de seguimento e séries com milhares de pacientes (registros internacionais, séries de Lyon, UCL/Londres, Heidelberg), os resultados consolidados em pacientes adequadamente selecionados mostram:
Sobrevida Câncer-Específica em 10 Anos
> 95-99% em pacientes com câncer de risco baixo a intermediário favorável, adequadamente selecionados — comparável à cirurgia e radioterapia.
Sobrevida Livre de Tratamento Adicional
- Em 5 anos: 70-85% — ou seja, 15-30% precisam de retratamento (re-HIFU, cirurgia ou radioterapia).
- Em 10 anos: 60-75%.
Sobrevida Livre de Falha Bioquímica (Critério Phoenix)
- Em 5 anos: 70-85% conforme risco.
- Em 10 anos: 55-70%.
Comparação com Prostatectomia e Radioterapia
Não há estudos randomizados grandes comparando diretamente HIFU com cirurgia ou radioterapia. As comparações observacionais (com limitações metodológicas) sugerem resultados oncológicos comparáveis em câncer de risco baixo a intermediário favorável, com perfil funcional significativamente melhor com HIFU.
Estudo HIFI (França, Crouzet e cols.)
Maior série prospectiva publicada — milhares de pacientes seguidos por mais de 10 anos. Demonstrou:
- Boa sobrevida câncer-específica.
- Taxa de retratamento aceitável.
- Preservação significativa da função urinária e sexual.
Registro Internacional de HIFU
Dados consolidados de múltiplos centros mostram resultados reproduzíveis em pacientes bem selecionados, com curva de aprendizado importante no centro tratante.
10. Resultados Funcionais: A Maior Vantagem do HIFU
Aqui está o principal motivo pelo qual o HIFU existe — e sua maior força:
Continência Urinária
Preservada em >95% dos pacientes. A maioria não desenvolve incontinência clinicamente significativa após HIFU focal ou hemiablação. Ocasionalmente há urgência miccional transitória nas primeiras semanas — geralmente resolutiva.
Função Erétil
Preservada em 70-85% dos pacientes adequadamente selecionados (com função basal boa e técnica nerve-sparing aplicável). Compare com 40-60% após prostatectomia bilateral nerve-sparing em centros experientes.
Ejaculação
Frequentemente preservada (parcial ou totalmente), diferente da prostatectomia (onde é perdida definitivamente). Pode haver redução do volume ejaculado conforme a extensão da ablação.
Função Intestinal
Praticamente sem alteração quando o procedimento é bem executado com preservação retal adequada.
Qualidade de Vida Global
Múltiplos estudos com questionários validados (EPIC-26, SF-36) mostram melhor preservação de qualidade de vida após HIFU comparado a opções radicais, especialmente nas dimensões sexual e urinária.
11. Complicações e Riscos: O Que Pode Acontecer
Como qualquer procedimento, o HIFU tem riscos. A maioria é leve e autolimitada, mas complicações graves existem e precisam ser conhecidas.
Complicações Leves (Comuns, Geralmente Autolimitadas)
- Hematúria transitória (primeiros dias).
- Urgência miccional, polaciúria (primeiras semanas).
- Desconforto perineal (primeiros dias).
- Sangramento retal leve (raro, autolimitado).
- Eliminação de fragmentos teciduais pela urina (primeiros meses).
Complicações Moderadas (Manejáveis)
- Retenção urinária aguda após retirada da sonda (3-5%) — geralmente resolve com sondagem temporária e medicação.
- Estenose de uretra ou colo vesical (3-8% em alguns estudos) — pode requerer dilatação endoscópica ou outras intervenções.
- Disfunção erétil parcial transitória — geralmente recuperável com reabilitação peniana.
- Infecção urinária pós-procedimento — tratada com antibióticos.
Complicações Graves (Raras, mas Importantes)
- Fístula uretrorretal (<1%) — comunicação anormal entre uretra e reto. Complicação séria, exige tratamento cirúrgico complexo. Praticamente eliminada com técnica moderna e indicação correta.
- Incontinência urinária significativa (1-3%) — mais provável quando há tratamento extenso ou lesão próxima ao esfíncter.
- Necrose tecidual extensa com complicações secundárias — raro.
Taxa Geral de Complicações Graves
Em mãos experientes, com indicação adequada: < 2-3%.
A experiência do centro e a indicação criteriosa são os fatores que mais reduzem a chance de complicação grave.
12. Quando o HIFU Não Funciona: Opções de Resgate
Em 15-30% dos pacientes, o HIFU não controla definitivamente a doença e algum tipo de retratamento é necessário. Saber as opções de resgate é parte de uma decisão informada.
Re-HIFU (HIFU Repetido)
Possível em casos selecionados — nova ablação focal ou em outra área. Boa opção quando a recidiva é local, pequena e bem caracterizada.
Prostatectomia de Salvamento
Cirurgia para remoção da próstata após HIFU. Tecnicamente mais difícil do que prostatectomia primária — fibrose induzida pelo HIFU altera planos cirúrgicos. Maior risco de incontinência e disfunção erétil pós-operatória, mas viável em mãos experientes.
Radioterapia de Salvamento
Pode ser indicada quando a recidiva é local sem condições para nova ablação focal. Estratégia bem estabelecida.
Crioterapia ou NanoKnife de Salvamento
Em centros experientes, outras modalidades focais podem ser usadas como salvamento, dependendo do cenário.
Tratamento Sistêmico
Para casos com progressão para doença avançada, hormonioterapia e outras terapias sistêmicas entram em cena.
A escolha do tratamento de resgate depende da localização e extensão da recidiva, do tempo desde o HIFU, do estado funcional do paciente e da experiência do centro.
13. HIFU x Outras Opções: Como Se Posiciona em 2026
HIFU vs Vigilância Ativa
- Vigilância ativa é para câncer de baixo risco bem caracterizado, sem necessidade imediata de tratamento.
- HIFU é para pacientes com câncer significativo identificado que precisa ser tratado — mas que não precisaria (ou não querem) tratamento radical do órgão inteiro.
HIFU vs Prostatectomia Radical
- Cirurgia: maior chance de cura definitiva, retira a próstata inteira, permite estadiamento patológico definitivo. Risco maior de incontinência e disfunção erétil.
- HIFU: preservação funcional dramática, sem incisões, recuperação rápida. Necessita seguimento mais intenso e pode requerer retratamento.
HIFU vs Radioterapia
- Radioterapia: trata toda a próstata, sem incisões, várias semanas de tratamento (ou 5 sessões em SBRT). Efeitos urinários, intestinais e sexuais podem ser tardios e cumulativos.
- HIFU: uma sessão única, sem radiação. Cirurgia ou radioterapia de resgate são mais factíveis depois de HIFU do que depois de radioterapia.
HIFU vs Crioterapia / NanoKnife
- Crioterapia: funciona em próstatas calcificadas onde HIFU é limitado; útil como salvamento pós-radioterapia.
- NanoKnife (IRE): mecanismo não térmico, ideal para lesões próximas a estruturas críticas (uretra, esfíncter, nervos).
- HIFU: maior maturidade, mais dados de longo prazo, plataformas modernas com fusão de imagem.
Nenhuma é "a melhor" — são opções com perfis distintos para pacientes distintos.
14. Quanto Custa e Onde Fazer HIFU no Brasil
Disponibilidade
O HIFU está disponível no Brasil em centros de referência em grandes capitais (São Paulo, Rio de Janeiro, Brasília, Porto Alegre, Belo Horizonte e outras). A disponibilidade varia conforme a plataforma (Sonablate, Focal One, Ablatherm).
Cobertura por Planos de Saúde
A cobertura é limitada e variável. Em situações específicas (indicação estritamente dentro de critérios consagrados), alguns planos cobrem com justificativa clínica detalhada. Em outros casos, a via é particular ou via NATJUS/ação judicial. A discussão prévia com a equipe e o convênio é essencial.
Custo Particular
Varia conforme o centro, plataforma utilizada, hospital e equipe. Pode estar na faixa de dezenas de milhares de reais, geralmente em valores comparáveis aos da cirurgia robótica particular.
Como Escolher o Centro
Critérios objetivos:
- Volume cirúrgico do urologista em HIFU (curva de aprendizado é importante).
- Plataforma disponível (Sonablate, Focal One, Ablatherm — cada uma com vantagens).
- Integração com radiologia experiente em mpMRI e biópsia por fusão.
- Protocolo estruturado de seguimento pós-HIFU.
- Capacidade de oferecer tratamento de resgate se necessário (cirurgia, radioterapia, re-HIFU).
15. O Futuro do HIFU: Para Onde Caminha a Tecnologia
A evolução nos próximos 5-10 anos deve incluir:
HIFU guiado por ressonância em tempo real (plataformas como Focal One e TULSA-PRO) — controle dosimétrico ainda mais preciso.
Inteligência artificial para planejamento personalizado e previsão de resposta.
Biomarcadores genômicos (Decipher, Oncotype, Prolaris) para refinar a seleção de candidatos.
Combinações com radioterapia, hormonioterapia ou imunoterapia em cenários selecionados.
Padronização internacional de critérios de falha bioquímica e definições de sucesso.
Indicações ampliadas para perfis hoje considerados marginais (alguns risco intermediário desfavorável, doença oligometastática local).
O HIFU em 2030-2035 provavelmente será muito mais preciso, mais personalizado e indicado para perfis específicos com base em assinatura molecular individual.
16. Perguntas Frequentes Sobre HIFU (FAQ Completo)
O HIFU é cirurgia?
Não no sentido tradicional. Não há cortes, incisões, nem remoção física de tecido. É um procedimento minimamente invasivo realizado por via transretal, sob anestesia, em ambiente cirúrgico — mas sem cirurgia aberta nem laparoscópica.
O HIFU dói?
Durante o procedimento, não — você está sob anestesia geral ou raquianestesia. No pós-operatório, há desconforto perineal leve a moderado controlado com analgésicos comuns. A maioria dos pacientes descreve a recuperação como mais confortável do que esperavam.
Quanto tempo de internação é necessário?
Geralmente alta no mesmo dia ou em 24 horas. Sonda vesical mantida por 5-10 dias após o procedimento.
Quando volto a trabalhar e dirigir?
A maioria dos pacientes retorna a atividades leves e ao trabalho em 7-14 dias. Dirigir é geralmente liberado após a retirada da sonda. Esforço físico intenso geralmente liberado em 3-4 semanas.
Posso ter ereção depois do HIFU?
Sim, na maioria dos pacientes (70-85% mantêm função erétil), especialmente quando há boa função basal e técnica que preserva os feixes neurovasculares. Pode haver alteração transitória nas primeiras semanas por edema local.
Vou ficar incontinente?
A continência é preservada em mais de 95% dos pacientes. Risco de incontinência clinicamente significativa é baixo (1-3%) e relaciona-se a ablações próximas ao esfíncter.
Vou perder a ejaculação?
Não necessariamente. Diferente da prostatectomia (perda definitiva), o HIFU frequentemente preserva ejaculação, embora possa haver redução de volume conforme a extensão tratada.
O HIFU cura o câncer de próstata?
Em pacientes adequadamente selecionados, oferece controle oncológico comparável à cirurgia e radioterapia em câncer de risco baixo a intermediário favorável, com sobrevida câncer-específica em 10 anos superior a 95-99%. Mas 15-30% precisam de algum retratamento ao longo do tempo.
Posso fazer HIFU mais de uma vez?
Sim. O HIFU pode ser repetido (re-HIFU) em casos selecionados de recidiva local. É uma das suas vantagens — permite estratégia de tratamentos sequenciais focais antes de partir para opções radicais.
O HIFU é coberto pelo plano de saúde?
Cobertura é limitada e varia por convênio. Algumas indicações específicas têm cobertura com justificativa clínica detalhada; outras seguem via particular ou recurso administrativo. Sempre confirme antes de programar.
Posso fazer cirurgia depois se o HIFU falhar?
Sim, mas a cirurgia de salvamento é tecnicamente mais difícil após HIFU, com maior risco de incontinência e disfunção erétil pós-operatória do que cirurgia primária. Por isso a seleção inicial é tão crítica.
O HIFU pode tratar câncer em qualquer parte da próstata?
Lesões em região posterior, lateral e ápice são as mais acessíveis ao HIFU transretal. Lesões muito anteriores em próstatas grandes podem estar fora do alcance — nesse caso, outras modalidades focais (NanoKnife, TULSA) ou tratamento radical podem ser melhores.
O que é PSMA-PET/CT e preciso fazer antes do HIFU?
PSMA-PET/CT é um exame de medicina nuclear que detecta doença em todo o corpo. Não é rotina antes de HIFU em câncer localizado de baixo-intermediário risco, mas pode ser solicitado em casos selecionados (risco mais alto ou suspeita de doença extra-prostática) para garantir que o HIFU é apropriado.
Quantos anos o HIFU "dura"?
Não há um "prazo de validade". Os resultados oncológicos são durables, com 10-15 anos de seguimento publicado mostrando bons desfechos em pacientes selecionados. O seguimento é vitalício, com PSA e imagem periódicos.
O HIFU está disponível no SUS?
Não como rotina, embora alguns centros públicos de referência venham incorporando a tecnologia. Atualmente a maioria do acesso é por planos de saúde (parcial) ou particular.
Conclusão
O HIFU para câncer de próstata em 2026 é uma realidade clínica madura, com mais de uma década de evidência consolidada, reconhecida pelas principais diretrizes mundiais como opção válida para pacientes adequadamente selecionados. Para o paciente certo — câncer unilateral ou unifocal, lesão índice bem caracterizada, risco baixo a intermediário favorável, função basal preservada e disposição para seguimento rigoroso — oferece um caminho com controle oncológico semelhante ao da cirurgia e da radioterapia, com preservação funcional dramaticamente superior.
Mas o HIFU não é mágica nem solução universal. Exige seleção rigorosa, equipe experiente, plataforma moderna e seguimento estruturado por anos. Indicado para o paciente errado, perde seus benefícios e pode comprometer tratamentos futuros. A escolha do centro e do cirurgião importa tanto quanto a escolha da técnica.
Se você tem câncer de próstata localizado e está pesquisando alternativas a cirurgia, radioterapia ou vigilância ativa, o HIFU pode (ou não) ser a melhor opção para o seu caso. A única forma de saber com clareza é avaliação especializada multidisciplinar, com mpMRI atualizada, biópsia direcionada por fusão e discussão honesta sobre todas as opções disponíveis — incluindo as situações em que o HIFU não é a melhor escolha.
Decida com informação completa, dados reais e equipe que conheça profundamente todas as opções terapêuticas, não apenas a que mais oferece.
Avaliação Para Indicação de HIFU
Você tem diagnóstico de câncer de próstata localizado e quer saber se o HIFU pode ser uma opção real para o seu caso? A elegibilidade depende de fatores específicos — e a decisão precisa ser tomada com avaliação multidisciplinar honesta.
👉 [Clique aqui para agendar sua consulta]
📱 [Clique aqui para falar com equipe]
"HIFU não é tratamento para todos. É tratamento certo para alguns. A diferença entre os dois cenários está na qualidade da avaliação prévia — não na propaganda da técnica."
Sobre o Autor
Dr. Alexandre Sato — Urologista | Uro-Oncologista
Médico urologista com formação dedicada à uro-oncologia e ao manejo integral do câncer de próstata em todas as fases. Trabalho com avaliação imparcial e individualizada das opções terapêuticas — incluindo vigilância ativa, tratamento focal (HIFU, crioterapia, NanoKnife), cirurgia robótica/laparoscópica e radioterapia — sempre com o objetivo de oferecer ao paciente o tratamento certo para seu caso, e não apenas o tratamento que estou tecnicamente mais inclinado a fazer.
Acompanho pacientes em todas as etapas da jornada — do diagnóstico inicial com mpMRI e biópsia direcionada por fusão MRI/US, passando pela decisão terapêutica multidisciplinar, até o seguimento estruturado de longo prazo e manejo de eventual recidiva (incluindo cirurgia de salvamento após HIFU ou radioterapia, quando indicada).
Comentários0
Ninguém escreveu ainda. Comente primeiro!
Envie suas Dúvidas e Comentários

Dr. Alexandre Sato
Médico Urologista em São Paulo - SP
A Begin Clinic é uma clínica especializada em tratamentos de reprodução assistida na cidade de São Paulo - SP. Também atendemos pacientes de outras cidades e estados em todo Brasil e exterior, que buscam por tratamentos de excelência, com médicos especialistas em congelamento de óvulos.
Saiba mais sobre Dr. Alexandre Sato.
CRM-SP: 146.210 - RQE: 61330
Curriculum Lattes: http://lattes.cnpq.br/6551764447584301