Câncer de bexiga: sintomas, causas, diagnóstico e tratamento ? guia completo 2026
Introdução
O câncer de bexiga é o 9º tumor maligno mais incidente do mundo e o segundo mais comum do aparelho urinário, atrás apenas do câncer de próstata. No Brasil, o INCA estima cerca de 12.000 novos casos por ano, com predomínio em homens acima de 60 anos e em grandes fumantes. Apesar de menos divulgado do que o câncer de mama ou de próstata, é uma doença altamente tratável quando diagnosticada cedo — e, em contrapartida, das mais agressivas quando negligenciada.
Este guia reúne, em linguagem clara e embasada nas diretrizes da American Urological Association (AUA/SUO 2023), European Association of Urology (EAU 2024), Sociedade Brasileira de Urologia (SBU) e nos estudos de referência publicados em 2024–2025, tudo o que pacientes, familiares e cuidadores precisam saber para entender, decidir e se tratar.
O que é o câncer de bexiga
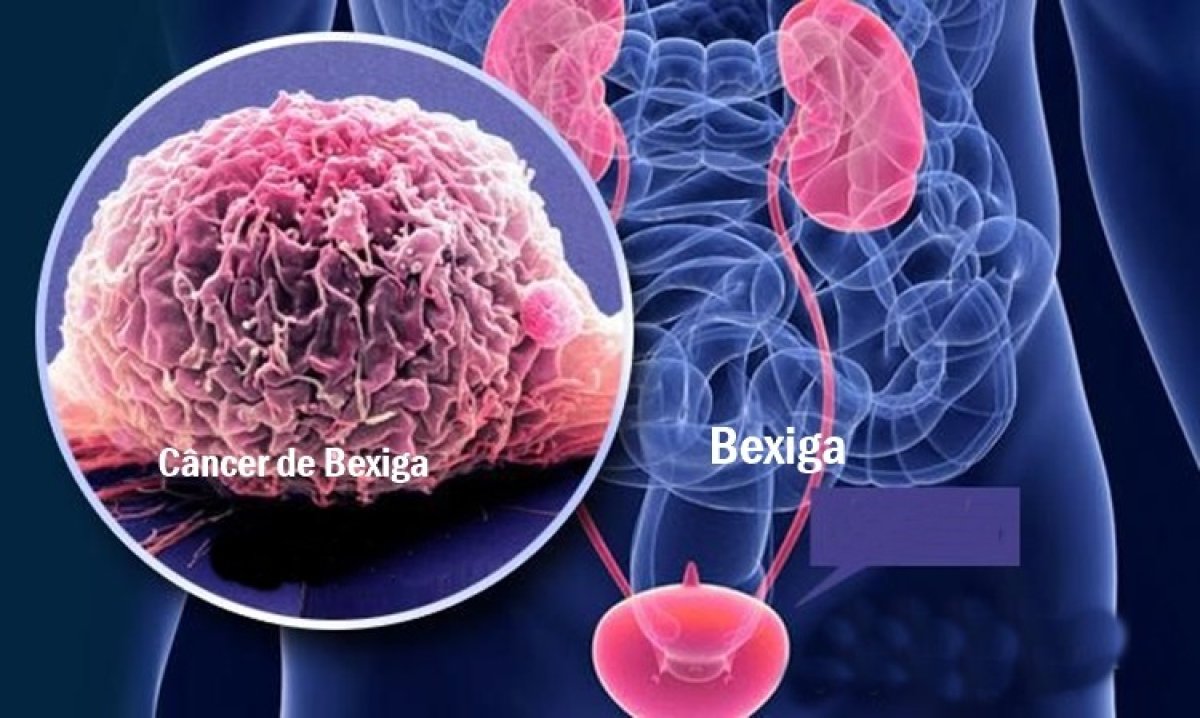
A bexiga é um órgão muscular oco, localizado na pelve, cuja função é armazenar e liberar a urina. Sua parede tem quatro camadas (urotélio, lâmina própria, músculo detrusor e gordura perivesical). O câncer de bexiga surge quando células do urotélio — a camada mais interna, em contato direto com a urina — sofrem mutações e passam a se multiplicar sem controle.
Tipos histológicos
- Carcinoma urotelial (90–95%) — o mais comum, originado do epitélio transicional
- Carcinoma de células escamosas (3–7%) — mais frequente em áreas endêmicas de esquistossomose urinária
- Adenocarcinoma (1–2%) — raro, frequentemente associado a remanescentes embrionários (úraco)
- Carcinoma de pequenas células / neuroendócrino (<1%) — raro, altamente agressivo
- Variantes histológicas — micropapilar, plasmocitóide, sarcomatóide, em ninhos — mais agressivas, exigem abordagem diferenciada
Dois grandes grupos clínicos
O câncer de bexiga se divide clinicamente em dois universos com tratamento e prognóstico radicalmente distintos:
- NMIBC — Não Músculo-Invasivo (Ta, T1, Tis/CIS) — 75–80% dos casos, geralmente curável com tratamento endoscópico e intravesical
- MIBC — Músculo-Invasivo (T2–T4) — 20–25% dos casos, exige tratamento multimodal agressivo
Essa divisão é o ponto mais importante de todo o artigo: é o que decide se a bexiga pode ser preservada ou se a cirurgia radical é necessária.
Causas e fatores de risco
Tabagismo — o fator #1
O tabagismo é responsável por 50% dos casos em homens e 30% em mulheres. Fumantes têm 3 a 5 vezes mais risco do que não fumantes, proporcional à carga tabágica (maços/ano). As aminas aromáticas e nitrosaminas do cigarro são excretadas pela urina e permanecem em contato prolongado com o urotélio. O cigarro eletrônico (vape) também contém carcinógenos urotéliotrópicos — em menor quantidade, porém em concentrações mais elevadas que o ambiente basal.
Exposição ocupacional
Profissionais historicamente em risco elevado:
- Pintores, trabalhadores de tintas e corantes
- Trabalhadores da indústria de borracha, couro e tecidos
- Metalúrgicos expostos a hidrocarbonetos aromáticos
- Cabeleireiros (exposição crônica a tinturas)
- Frentistas e trabalhadores de refinarias
- Trabalhadores de fundição e alumínio
Outros fatores
- Idade — risco aumenta após os 55 anos
- Sexo masculino — 3 a 4x mais frequente que em mulheres
- Radioterapia pélvica prévia (câncer de próstata, colo uterino, reto)
- Ciclofosfamida (quimioterapia e imunossupressão crônica)
- Esquistossomose urinária (Schistosoma haematobium) — em áreas endêmicas
- Infecções urinárias de repetição
- Cistite crônica e uso prolongado de sonda vesical
- Histórico familiar de câncer urotelial
- Síndrome de Lynch (câncer colorretal hereditário não poliposo)
- Arsênio na água (regiões específicas)
Sinais e sintomas
O sintoma #1: hematúria
Sangue visível na urina (hematúria macroscópica) é o sintoma mais frequente e ocorre em 75–85% dos pacientes. Importante:
- É tipicamente indolor
- Pode ser intermitente (o paciente "alivia" com a normalização e adia a investigação — erro crítico)
- Pode ser terminal (no fim do jato), inicial ou total
- Qualquer hematúria macroscópica em adulto — mesmo uma única vez — é investigação urgente
A hematúria microscópica (vista apenas ao exame de urina) também pode ser manifestação, embora com valor preditivo menor.
Sintomas irritativos
- Urgência miccional
- Aumento da frequência urinária
- Ardência ao urinar
- Dor suprapúbica
Costumam ser confundidos com infecção urinária de repetição — especialmente em mulheres. Nos casos de CIS (carcinoma in situ), os sintomas irritativos dominam o quadro, sem hematúria visível.
Sintomas de doença avançada
- Perda de peso inexplicada
- Dor lombar (sinal de hidronefrose por invasão ureteral)
- Massa pélvica palpável
- Edema de membros inferiores
- Dor óssea (metástases)
Diagnóstico
O processo diagnóstico combina anamnese, exames de imagem, laboratoriais e confirmação histológica.
Exames iniciais
- Exame de urina (EAS/Urina tipo I) — confirma hematúria
- Urocultura — exclui infecção
- Citologia urinária — detecta células atípicas, útil principalmente em CIS e alto grau
- Ultrassom das vias urinárias — boa sensibilidade para tumores maiores
- Função renal (creatinina, ureia) — orienta uso de contraste
Exames de imagem de estadiamento
- Uro-tomografia computadorizada (uro-TC) com contraste — exame padrão para avaliação do trato urinário superior e da pelve
- Ressonância multiparamétrica da bexiga com VI-RADS — ferramenta cada vez mais utilizada para predizer invasão muscular antes da RTU
- PET-CT com FDG — casos selecionados, principalmente suspeita de metástases
- Cintilografia óssea — se houver dor óssea ou fosfatase alcalina elevada
Cistoscopia — o exame que fecha o diagnóstico
A cistoscopia permite visualizar diretamente o interior da bexiga. É o exame-padrão para suspeita de câncer de bexiga. Pode ser:
- Diagnóstica — feita em ambulatório, com anestesia tópica
- Com luz branca tradicional
- Com técnicas avançadas — PDD (fotodinâmica com hexil-aminolevulinato, "luz azul") e NBI (narrow band imaging), que aumentam a detecção de lesões planas como o CIS
Quando há suspeita, prossegue-se para a RTU de bexiga (RTUB/TURBT) sob anestesia, que simultaneamente confirma o diagnóstico (biópsia) e remove o tumor.
Biomarcadores urinários (complementares)
- NMP22, BTA, UroVysion, CxBladder, EpiCheck, Xpert Bladder Cancer -Ainda não disponíveis no Brasil.
São úteis no seguimento de pacientes com NMIBC de alto risco, ainda não substituindo a cistoscopia, mas podendo complementá-la.
Estadiamento e classificação
O sistema TNM (AJCC 8ª edição) define a extensão da doença.
T (profundidade)
- Ta — papilífero restrito ao urotélio → NMIBC
- Tis (CIS) — plano, alto grau, intraepitelial → NMIBC
- T1 — invade a lâmina própria → NMIBC
- T2 — invade o músculo detrusor → MIBC
- T3 — invade a gordura perivesical → MIBC
- T4 — invade órgãos adjacentes → MIBC
Grau histológico (OMS 2016)
- Baixo grau (LG) — menor agressividade
- Alto grau (HG) — maior risco de progressão
Estratificação de risco do NMIBC (EAU 2024)
Baixo, intermediário, alto e muito alto risco — orientam tratamento intravesical e frequência de seguimento.
📌Para leitura aprofundada, veja nosso artigo: "Tumor de bexiga NMIBC x MIBC: entenda a diferença que decide seu tratamento".
Tratamento por estágio
Tratamento do NMIBC
1. RTU de bexiga (RTUB/TURBT) — sempre o primeiro passo. Remove o tumor, fornece amostra para diagnóstico e estadiamento.
2. Instilação intravesical precoce — dose única de mitomicina C ou gencitabina nas primeiras 6–24h, em casos selecionados.
3. BCG intravesical (imunoterapia) — padrão-ouro para alto risco e CIS. Indução (6 doses) + manutenção por 1 a 3 anos.
4. Quimioterapia intravesical — mitomicina, gencitabina ou docetaxel, em intermediários ou falha do BCG.
5. Re-RTU (second look) — obrigatória em T1, tumores grandes/múltiplos ou ausência de músculo detrusor.
6. Cistectomia radical precoce — em NMIBC de muito alto risco ou falha/intolerância ao BCG.
📌Veja nossos artigos: "Como é o pré-operatório da RTU de bexiga" e "Pós-operatório da RTU de bexiga".
Tratamento do MIBC
1. Quimioterapia neoadjuvante — MVAC dose-densa ou gencitabina + cisplatina em pacientes aptos. Aumenta sobrevida global em 5–8% em 5 anos.
2. Cistectomia radical com linfadenectomia pélvica estendida — retirada da bexiga, próstata e vesículas seminais (homens) ou útero, anexos e parede vaginal anterior (mulheres), com reconstrução urinária.
3. Derivações urinárias:
- Neobexiga ortotópica (Studer, Hautmann) — bexiga artificial construída com intestino
- Conduto ileal (Bricker) — estoma cutâneo
- Indiana pouch — reservatório continente cateterizável
4. Tratamento trimodal (preservação da bexiga) — RTU máxima + quimioterapia + radioterapia, em pacientes selecionados. Resultados comparáveis à cistectomia em casos bem indicados.
5. Imunoterapia adjuvante — nivolumabe (estudo CheckMate-274) por 1 ano em pacientes com alto risco de recidiva pós-cirurgia.
Tratamento da doença metastática
O cenário foi transformado pelas novas terapias:
- Enfortumabe vedotina + pembrolizumabe — primeira linha padrão desde o estudo EV-302 (NEJM, 2023), superando a quimioterapia clássica em sobrevida
- Quimioterapia baseada em platina — cisplatina ou carboplatina + gencitabina
- Imunoterapia em monoterapia — pembrolizumabe, atezolizumabe, nivolumabe, avelumabe (manutenção)
- Terapias-alvo — erdafitinibe em tumores com alterações FGFR
Seguimento após tratamento
O câncer de bexiga é a neoplasia urológica que mais recidiva. O seguimento é parte integral do tratamento.
Seguimento do NMIBC
- Cistoscopia a cada 3 meses no primeiro ano
- Cistoscopia a cada 6 meses até o 2º ano
- Cistoscopia anual por até 10 anos (muitas vezes vitalícia)
- Citologia urinária associada em alto risco
- Uro-TC ou uro-RM periódicos no alto risco
Seguimento do MIBC pós-cistectomia
- Tomografia de tórax, abdome e pelve a cada 6 meses por 3 anos, depois anual
- Exames laboratoriais (função renal, hemograma, B12) — importantes em portadores de neobexiga
- Cistoscopia da uretra remanescente em alguns casos
- Avaliação de continência e função sexual
Prognóstico e sobrevida
NMIBC
- Baixo risco: sobrevida câncer-específica > 95% em 5 anos
- Risco intermediário: 85–90%
- Alto risco: 65–85%
- Muito alto risco: 50–70%
MIBC
- Localizado (T2N0): 50–65% em 5 anos
- T3/T4 localizado: 30–50%
- Linfonodos positivos: 15–30%
- Metástase à distância: historicamente mediana de 12–15 meses — com novas imunoterapias, sobrevida mediana em 2024 ultrapassa 30 meses em pacientes tratados com EV + Pembro
Prevenção
Medidas com impacto comprovado
- Não fumar e não vaporizar — o fator isolado mais importante
- Parar de fumar — reduz risco em ≈30% em 4 anos e ≈50% em 10 anos
- Proteção ocupacional — EPI adequado em pintores, metalúrgicos, cabeleireiros, frentistas
- Hidratação adequada (2 L/dia) — reduz tempo de contato de carcinógenos com o urotélio
- Dieta rica em frutas, vegetais crucíferos e pobre em carnes processadas
- Investigar precocemente hematúria — o tempo entre o sintoma e o diagnóstico é determinante
Rastreamento
Não há recomendação de rastreamento populacional — mas exame de urina e avaliação urológica periódica são recomendados em pacientes de alto risco (tabagistas pesados, expostos ocupacionais, história familiar).
Perguntas Frequentes :
- Qual é o principal sintoma do câncer de bexiga? Sangue visível na urina (hematúria macroscópica) indolor e intermitente, em 75–85% dos casos. Qualquer episódio em adulto exige investigação urgente.
- Todo sangue na urina é câncer de bexiga? Não. Pode ser causado por infecção, pedras, trauma, medicações ou doenças da próstata. Porém, em adulto acima de 40 anos, deve sempre ser investigado com cistoscopia e imagem.
- Câncer de bexiga tem cura? Sim, especialmente o NMIBC, com taxas de sobrevida câncer-específica superiores a 85%. O MIBC tem cura em 45–65% dos casos localizados e depende de tratamento multimodal rápido e qualificado.
- Qual é o principal fator de risco do câncer de bexiga? Tabagismo (ativo ou passado), responsável por 50% dos casos em homens e 30% em mulheres. Exposição ocupacional a aminas aromáticas é o segundo fator mais relevante.
- Cigarro eletrônico (vape) também aumenta o risco de câncer de bexiga? Sim. O vape contém carcinógenos urotéliotrópicos (aminas aromáticas, acroleína, nitrosaminas) em menores quantidades que o cigarro, mas acima do basal. Considera-se de risco reduzido, porém não nulo.
- Como é feito o diagnóstico do câncer de bexiga? Combinação de exame de urina, ultrassom, uro-TC ou ressonância, citologia urinária e cistoscopia com biópsia (RTU de bexiga), que fecha o diagnóstico histológico.
- Preciso sempre retirar a bexiga para tratar câncer de bexiga? Não. 75% dos casos são NMIBC e tratados preservando a bexiga com RTU e BCG intravesical. A cistectomia radical é indicada em MIBC, NMIBC muito alto risco ou falha do BCG.
- O BCG intravesical é quimioterapia? Não. É uma imunoterapia intravesical — deriva do bacilo da tuberculose (BCG) e estimula a resposta imune local contra as células tumorais. É o tratamento-padrão no NMIBC de alto risco.
- Quanto tempo dura o tratamento do câncer de bexiga? No NMIBC, 1 a 3 anos de BCG + seguimento cistoscópico por 10+ anos. No MIBC, 3 a 4 meses de quimioterapia + cirurgia + 1 ano de imunoterapia adjuvante, em casos indicados.
- Vivo sem bexiga: como é a qualidade de vida? Depende da derivação urinária escolhida. A neobexiga ortotópica permite urinar pela uretra de forma próxima ao natural. O Bricker utiliza estoma com bolsa externa. A qualidade de vida após 6–12 meses de adaptação costuma ser boa na maioria dos pacientes bem acompanhados.
Conclusão
O câncer de bexiga é uma doença muito mais tratável do que parece à primeira vista — desde que diagnosticada cedo, estadiada com precisão e conduzida por equipe experiente. Dois princípios orientam a abordagem moderna: hematúria nunca é trivial e a qualidade do primeiro tratamento (RTU ou cistectomia) determina o prognóstico dos próximos 20 anos. Com os avanços de 2023–2025 em imunoterapia, terapia-alvo e anticorpos conjugados, mesmo a doença avançada tem hoje opções que simplesmente não existiam há cinco anos. Em paralelo, o caminho mais eficaz continua sendo o mais simples: não fumar, não vaporizar, proteger-se no trabalho, investigar o sangue na urina e manter seguimento com urologista.
Diagnóstico, segunda opinião ou suspeita de câncer de bexiga?
Se você recebeu um diagnóstico de câncer de bexiga, apresenta hematúria inexplicada, sintomas urinários persistentes ou pertence a grupo de risco (fumante, usuário de vape, exposição ocupacional, histórico familiar), uma avaliação urológica especializada pode mudar seu prognóstico. Se busca segunda opinião para um plano cirúrgico ou oncológico já proposto, eu posso ajudar.
Analiso pessoalmente seus exames, revejo o laudo anatomopatológico, estratifico o risco conforme as diretrizes AUA/EAU e construo com você um plano terapêutico individualizado — do diagnóstico inicial ao seguimento oncológico de longo prazo.
Sobre o autor — Dr. Alexandre Sato
Dr. Alexandre Sato é urologista com dedicação ao tratamento cirúrgico e ao seguimento do câncer de bexiga, câncer de próstata e hiperplasia prostática benigna. Realiza rotineiramente RTU de bexiga (RTUB/TURBT), re-RTU (second look), cistectomia radical com derivações urinárias (neobexiga ortotópica, conduto ileal de Bricker e Indiana pouch), instilação intravesical com BCG e quimioterápicos (mitomicina, gencitabina, docetaxel), além de HoLEP e cirurgias urológicas minimamente invasivas.
Titulado pela Sociedade Brasileira de Urologia (SBU), fundamenta sua prática nas diretrizes da AUA (American Urological Association), EAU (European Association of Urology) e nos protocolos ERAS (Enhanced Recovery After Surgery). Mantém atualização contínua sobre as terapias de nova geração — imunoterapia (pembrolizumabe, nivolumabe, atezolizumabe), anticorpos conjugados (enfortumabe vedotina) e terapias-alvo (erdafitinibe).
Acredita que no câncer de bexiga o primeiro tratamento decide os próximos vinte anos — e por isso dedica-se à qualidade técnica da cirurgia, à precisão do estadiamento e à construção de seguimento oncológico disciplinado e humanizado.
Comentários0
Ninguém escreveu ainda. Comente primeiro!
Envie suas Dúvidas e Comentários

Dr. Alexandre Sato
Médico Urologista em São Paulo - SP
A Begin Clinic é uma clínica especializada em tratamentos de reprodução assistida na cidade de São Paulo - SP. Também atendemos pacientes de outras cidades e estados em todo Brasil e exterior, que buscam por tratamentos de excelência, com médicos especialistas em congelamento de óvulos.
Saiba mais sobre Dr. Alexandre Sato.
CRM-SP: 146.210 - RQE: 61330
Curriculum Lattes: http://lattes.cnpq.br/6551764447584301